Un système d’imagerie par cartographie optique pour mieux comprendre le fonctionnement du cerveau normal et pathologique
Mis à jour octobre 2024
Porteur du projet : Philippe LORY – Institut de Génomique Fonctionnelle (IGF – Montpellier)
Titre du projet : Cartographie optique des fonctions et maladies du cerveau
Équipement financé grâce à l’opération Rotary-Espoir en Tête 2022 et sélectionné par le Conseil Scientifique de la FRC : un système d’imagerie par cartographie optique pour un montant de 63 765 €
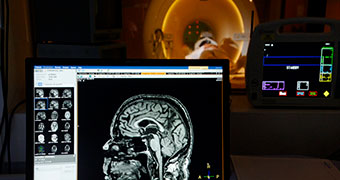
Description de l’équipement :
Le cerveau contrôle notre capacité à penser, à mémoriser, à parler, à ressentir, à voir, à entendre, à marcher, voire à respirer, et bien plus encore. Pour mieux comprendre l’organisation fonctionnelle du cerveau, les chercheurs doivent surveiller et analyser les activités électriques des neurones. Les neurones communiquent entre eux pour former des réseaux spécialisés et complexes. L’excitabilité est un processus à plusieurs niveaux, de l’activité d’un seul neurone à celle d’un réseau de neurones.
Décrypter les mécanismes d’excitabilité pour obtenir une vue d’ensemble de l’activité neuronale normale, du développement précoce au vieillissement, et de sa dérégulation dans les maladies neurologiques et psychiatriques fait l’objet des travaux de nombreux chercheurs de l’Institut de Génomique Fonctionnelle (IGF) à Montpellier. Si les techniques électrophysiologiques permettent d’interpréter de façon précise les signaux électriques d’un neurone, comme les variations du potentiel membranaire (potentiel électrique entre les deux faces d’une membrane cellulaire), ce sont les approches d’imagerie qui s’avèrent moins invasives et mieux adaptées pour l’étude de réseaux neuronaux, voire d’organismes entiers.
Implémenter à l’IGF de Montpellier une technique d’imagerie appelée « cartographie optique » permettra aux chercheurs de suivre à haute vitesse, sur des préparations neuronales multicellulaires et des organismes modèles, comment les variations dans le temps du potentiel de membrane déterminent la communication neuronale dans un environnement complexe (autres cellules, neuromodulateurs, …), en situation normale et dans divers modèles de maladies du système nerveux. Cette technique est l’avenir du suivi non invasif des événements électrophysiologiques dans les systèmes vivants, souvent inaccessibles aux méthodes basées sur les électrodes.
Le système identifié permet une acquisition d’images à grand champ et rapide. Ce système est plus couramment utilisé par les scientifiques du domaine cardiaque et quelque peu négligé dans le domaine des neurosciences. Il complètera un système avec lequel les chercheurs pourront enregistrer simultanément le potentiel membranaire et d’autres signaux biologiques (calcium, neurotransmetteurs, enzymes …).
11 projets de chercheurs de l’IGF, impliquant parfois des collaborations en dehors de l’IGF, bénéficieront tout particulièrement de cet équipement. En voici quelques exemples :
- Etude des réseaux de neurones dérivant de cellules souches de patients souffrant de maladies neurologiques, en particulier pour l’épilepsie, la maladie d’Alzheimer et l’atrophie cérébelleuse
- Etude de l’excitabilité neuronale sur des tranches de tissus humains, en particulier de moelle épinière.
- Etude du neurodéveloppement et de ses pathologies sur des larves de poissons zèbre.
- Effet de xénobiotiques (ex. pesticides) sur le neurodéveloppement
- Développement de nouveaux biosenseurs (ex. reporteurs ATP) pour l’étude des relations neurone-cellule gliale.
- Etude des altérations électriques à la jonction neuromusculaire de patients atteints d’amyotrophie spinale (SMA).
Ce système sera d’intérêt pour de nombreux projets de recherche en neurosciences et au-delà, en cardiologie entre autres.
Utilisation et intérêt de l’équipement
L’équipement a été mis en service en juin 2023 et mis à disposition de plusieurs équipes provenant de trois instituts de recherche différents.
L’exploration de l’activité électrique par cartographie optique permet de mieux comprendre comment et à quel moment cette activité se diffuse dans les tissus. En effet, si les approches classiques d’électrophysiologie par électrode en forme de micropipette permettent d’obtenir une connaissance précise de l’activité électrique sur une cellule appartenant à un tissu excitable, ou sur une cellule isolée du tissu, la cartographie optique permet de suivre l’évolution de ces phénomènes de façon globale, sur tout l’ensemble du tissu, ajoutant une dimension spatio-temporelle qui n’était pas possible avant.
Premiers résultats obtenus
Plusieurs projets en cours ont pu bénéficier de cet équipement qui permet un nouveau regard sur les dynamiques de l’activité électrique dans des tissus tels que le cerveau, le cœur et les muscles squelettiques. Parmi ces projets, l’analyse de l’activité cérébrale des modèles de poisson zèbre avec l’approche de cartographie optique s’est avérée essentielle pour analyser l’effet de pesticides, plastifiants et autres polluants sur leur physiologie. Grâce à cette nouvelle approche les chercheurs seraient en mesure de démontrer que l’exposition à des cocktails de pesticides et plastifiants, tels qu’ils se trouvent dilués dans les eaux en milieu naturel, affectent les fonctions cérébrales des poissons zèbre ainsi que des autres organismes, possiblement l’homme, exposé à ces contaminants.
Grâce à l’utilisation de cet équipement, des résultats ont été publiés dans une revue scientifique :
- High-speed optical mapping of heart and brain voltage activities in zebrafish larvae exposed to environmental contaminants, Environmental Technology & Innovation, Micou et al. 2023.
Prochaines utilisations
Les chercheurs vont continuer le projet ‘xénobiotique’ avec l’investigation des effets de plusieurs molécules sur l’activité cérébrale des larves des poissons zèbre. Ainsi, ils vont continuer des approches d’analyse de préparations cellulaires et tissulaires cérébrales et cardiaques. En parallèle, ils ont récemment ajouter un système permettant l’analyse de l’activité cardiaque sur cœur isolé avec perfusion continue.
Photographies : Inserm / équipe de Philippe Lory

Le chercheur
Philippe LORY est Directeur de Recherche CNRS à l’Institut de Génomique Fonctionnelle de Montpellier. Il y dirige l’équipe « Canaux ioniques – excitabilité neuronale et canalopathies« . Son expertise couvre la physiologie des canaux ioniques, leur régulation et les maladies génétiques liées à des mutations de ces canaux : les canalopathies, en particulier pour les canaux calciques. Les canalopathies calciques comprennent des formes d’épilepsie, de migraine, d’ataxie et d’autisme et d’autres formes encore de maladies du neurodéveloppement. Son laboratoire étudie les mécanismes pathogéniques responsables de ces maladies.
Témoignage du chercheur
« Je suis électrophysiologiste de formation, et avec l’électrophysiologie, nous avons pu décrypter les défauts électriques pour de nombreuses pathologies. L’épilepsie par exemple. Avec l’essor des approches en imagerie, nous pouvons maintenant examiner avec une très bonne dynamique temporelle d’autres signaux : le calcium, des neuromédiateurs libérés, des activités d’enzymes … et aussi les variations du potentiel de membrane. Autrement dit : nous pensons que les techniques d’imagerie rapide, telles que celles offertes par la cartographie optique, vont surmonter les limites des techniques électrophysiologiques en permettant d’examiner plusieurs signaux biologiques simultanément » – Philippe LORY

Le centre de recherche
Cet équipement sera installé au sein de l’Institut de Génomique Fonctionnelle (IGF) de Montpellier.